¿Puede Ozempic, Wegovy causar pérdida de cabello y ideación suicida? La FDA está investigando los efectos secundarios de los medicamentos GLP-1.
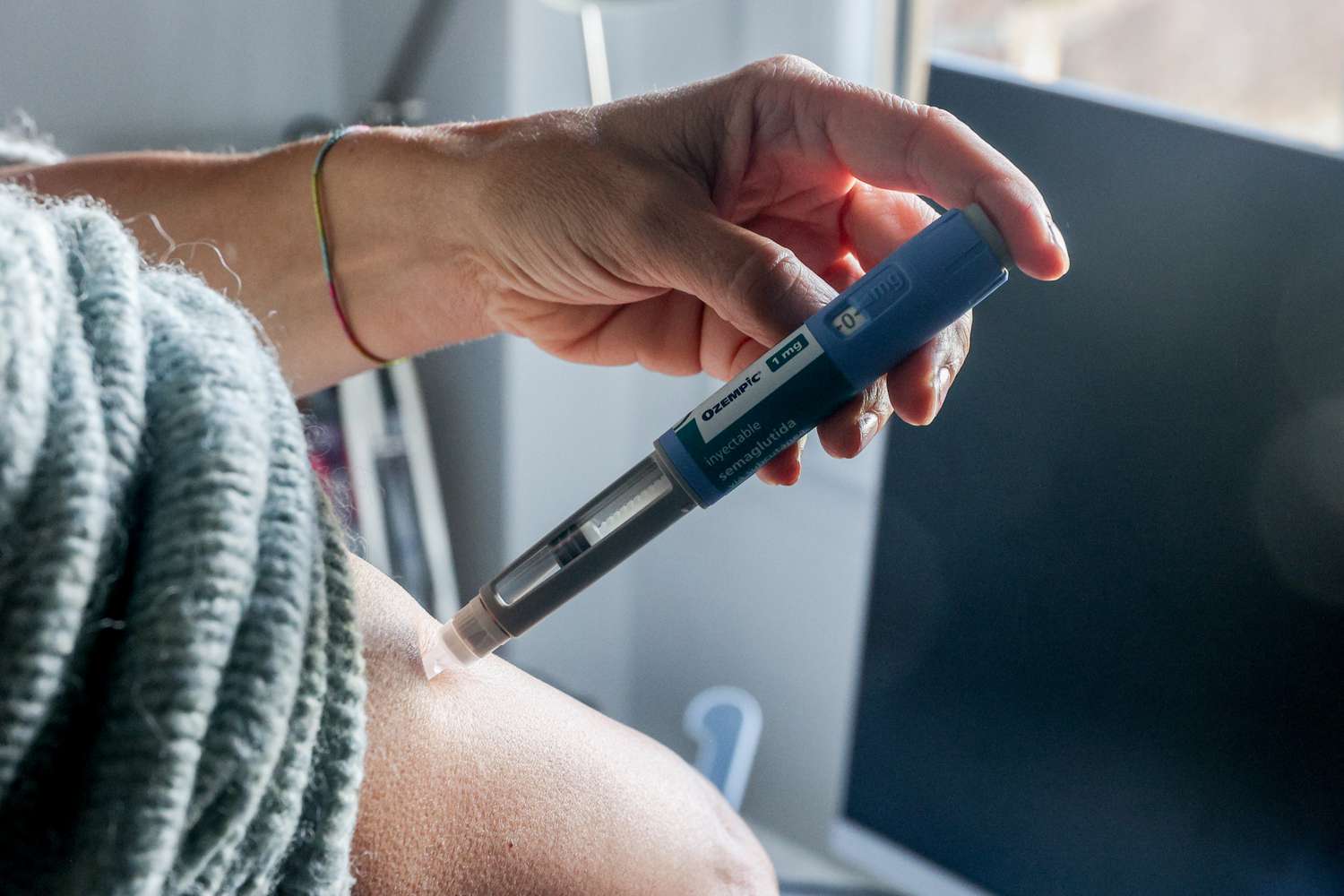
La Administración de Alimentos y Medicamentos (FDA) está examinando actualmente fármacos de uso generalizado como Ozempic y Wegovy debido a posibles asociaciones con ideación suicida, caída del cabello y aspiración.
Los informes de eventos adversos relacionados con los fármacos agonistas del receptor del péptido 1 similar al glucagón (GLP-1) se han presentado ante el Sistema de notificación de eventos adversos (FAERS) de la FDA. Estos medicamentos actualmente forman parte de una lista de revisión de la FDA, actualizada por última vez el 2 de enero.
Entre los medicamentos GLP-1 que se están considerando se encuentran los más nuevos, como Wegovy y Mounjaro, así como medicamentos más antiguos para la diabetes tipo 2 como Byetta, aprobado por primera vez en 2005.
Por el momento, la FDA sólo está "evaluando la necesidad de medidas regulatorias". A los fabricantes de medicamentos todavía no se les ha pedido que tomen ninguna medida, como actualizar las advertencias en las etiquetas de sus paquetes.
Este examen se produce unos seis meses después de que la Agencia Europea de Medicamentos (EMA) declarara que estaría revisando un posible vínculo entre los medicamentos GLP-1 y la ideación suicida, después de aproximadamente 150 informes sobre el tema.
Inicialmente se esperaba que la investigación concluyera en noviembre, pero el comité de la EMA presentó recientemente "listas adicionales de preguntas que deben abordarse" a las empresas que comercializan medicamentos GLP-1. Está previsto que el comité vuelva a examinar la cuestión en abril.
Además, un estudio publicado el 5 de enero examinó una posible asociación entre semaglutida (también conocida como Ozempic y Wegovy) y la ideación suicida. Se descubrió que estos medicamentos no tenían un mayor riesgo de pensamientos suicidas en comparación con otros medicamentos para la diabetes tipo 2 y para bajar de peso.
Mientras los funcionarios de salud y los investigadores continúan explorando los medicamentos GLP-1 y cualquier efecto secundario no incluido anteriormente, los expertos coinciden en que la revisión no debería causar alarma.
"Creo que [la revisión es] apropiada, ese es su objetivo regulatorio: garantizar la seguridad", dijo Holly Lofton, MD, directora del programa médico de control de peso de NYU Langone Health.
Aunque el sistema de informes adversos de la FDA identificó alopecia (pérdida de cabello), aspiración e ideación suicida, no prueba necesariamente que estos efectos secundarios fueron causados por los medicamentos.
Sin embargo, el sistema de revisión FAERS permite a la FDA monitorear cualquier problema de seguridad emergente, particularmente cuando un medicamento tiene un uso público generalizado.
“Estos efectos secundarios no se observaron en los ensayos clínicos, pero sólo afectan a unos 3.000 pacientes de ambos lados. En el mercado vivo, tratamos con millones de pacientes”, afirmó Ebne Rafi, PharmD, especialista en farmacia clínica del Centro de Diabetes y Obesidad de los Hospitales Universitarios de Cleveland.
Esta revisión es que la FDA “cumple con su deber”, explicó.
Aunque no existe un vínculo confirmado entre los medicamentos GLP-1 y los tres efectos secundarios identificados por la FDA, estudios previos han sugerido asociaciones.
La ideación suicida se ha asociado históricamente con los medicamentos para bajar de peso. Algunos medicamentos para bajar de peso incluso han sido retirados del mercado debido a un elevado riesgo de suicidio, dijo Lofton. Según Rafi, es probable que el impacto de los medicamentos para bajar de peso en el sistema nervioso central contribuya a este mayor riesgo.
Vale la pena señalar que la ideación suicida figura como una advertencia en la información de prescripción de Wegovy.
La caída del cabello y la pérdida de peso también están relacionadas. "La alopecia es uno de los efectos secundarios más recientes que se están investigando", mencionó Rafi. "La pérdida rápida de peso podría generar desequilibrios hormonales y cambios en un tipo particular de colágeno que, en algunos casos, pueden provocar la caída del cabello".
Este efecto se ha observado en personas que han experimentado una pérdida de peso significativa después de someterse a una gastrectomía en manga.
La relación entre los fármacos GLP-1 y la aspiración pulmonar (inhalación accidental de material que termina en los pulmones) es menos clara.
El Canadian Journal of Anesthesia advirtió en julio de 2023 sobre pacientes que inhalan inadvertidamente contenidos gástricos durante la cirugía porque sus estómagos no pueden vaciarse por completo. Hay investigaciones limitadas sobre el vínculo potencial entre los medicamentos GLP-1 y la ingestión accidental de alimentos en las vías respiratorias.
Por ahora, la FDA sólo está "evaluando la necesidad de medidas regulatorias", por lo que los cambios futuros en el uso de estos medicamentos, si los hay, siguen siendo inciertos.
Esta acción podría incluir "actualizar la información del etiquetado de un producto, restringir el uso del medicamento, comunicar nueva información de seguridad al público o, en casos excepcionales, retirar un producto del mercado".
Esta última opción es muy improbable en el caso de los fármacos GLP-1, coincidieron los expertos. Incluso si se demuestra que existe algún vínculo causal entre estos efectos secundarios y los medicamentos GLP-1, eso no necesariamente justificaría que no esté disponible, explicó Rafi.
“Por ejemplo, los medicamentos antidepresivos químicos tienen [el riesgo de ideación suicida] como advertencia importante. La mayoría de los medicamentos anticonvulsivos también”, dijo. "Y estos medicamentos han estado en el mercado durante años y años".
En todo caso, la FDA podría pedir a las empresas que actualicen sus etiquetas para incluir estos posibles efectos secundarios, dijeron los expertos. Esto acaba de suceder en octubre: la FDA añadió un efecto secundario gastrointestinal, el íleo, a la etiqueta de Ozempic.
En cuanto a por qué están surgiendo estas revisiones ahora, Lofton dijo que se debe en gran medida a la "gran masa de personas que están tomando algún tipo de estos medicamentos". En otras palabras, el número de eventos adversos está creciendo a medida que también aumenta el número de personas que toman el medicamento.
Aunque la revisión de la FDA es importante, no hay necesidad de que la gente se “estrese por ello”, especialmente cuando, por ahora, no existe un vínculo comprobado entre los medicamentos GLP-1 y la alopecia, la aspiración o la ideación suicida, dijo Rafi.
Esto es especialmente cierto para las personas que ya han tomado el medicamento y están viendo buenos resultados.
"Tengo muchos pacientes que vienen y han estado tomando estos medicamentos durante años conmigo, y dicen: 'Estoy muy preocupado por el íleo'. Y yo digo: 'Bueno, ¿tuviste íleo?' , No lo entendí." "Está bien, entonces no te preocupes", dijo Lofton.
Sin embargo, los pacientes o cualquier persona que esté considerando tomar Ozempic, Mounjaro o un medicamento relacionado deben ser conscientes de cualquier riesgo potencial y estar atentos a estos u otros efectos secundarios. Esto es especialmente cierto porque la experiencia de cada persona con el medicamento es diferente, añadió.
"Como proveedores, debemos asegurarnos de que los pacientes estén conscientes de los posibles efectos secundarios, especialmente los graves", dijo Lofton, "y luego hacer un seguimiento de los pacientes y asegurarnos de que nada adverso los ponga en un estado en el que corran más riesgo". que beneficio”.