Ozempic, Wegovy peuvent-ils causer la perte de cheveux et les idées suicidaires ? La FDA enquête sur les effets secondaires des médicaments GLP-1.
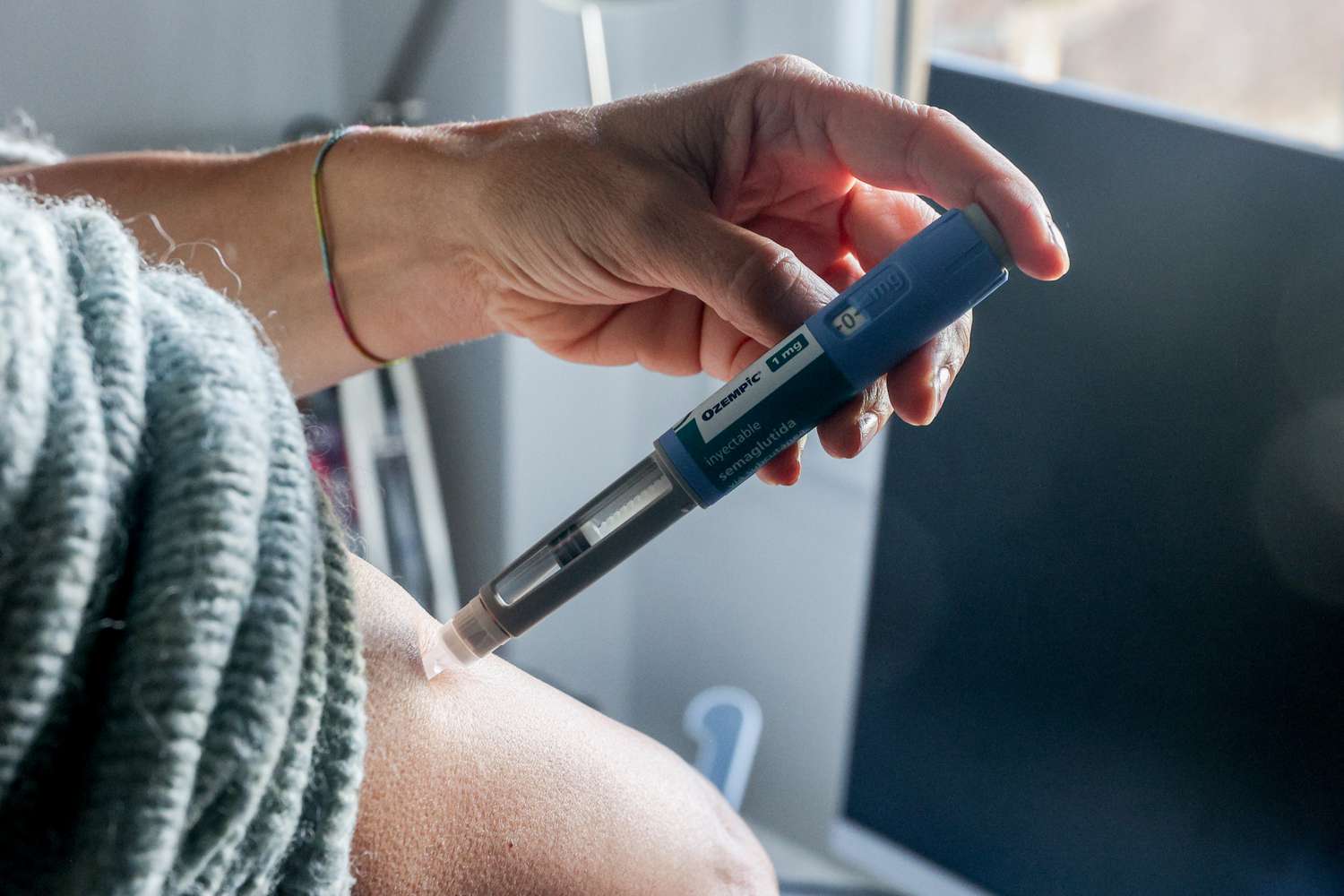
La Food and Drug Administration (FDA) examine actuellement des médicaments largement utilisés tels que Ozempic et Wegovy en raison d'associations potentielles avec des idées suicidaires, la perte de cheveux et l'aspiration.
Des rapports d’événements indésirables liés aux médicaments agonistes des récepteurs du Glucagon-like peptide-1 (GLP-1) ont été déposés auprès du Adverse Event Reporting System (FAERS) de la FDA. Ces médicaments font actuellement partie d’une liste d’examen de la FDA, mise à jour pour la dernière fois le 2 janvier.
Parmi les médicaments GLP-1 envisagés figurent des médicaments plus récents tels que Wegovy et Mounjaro, ainsi que des médicaments plus anciens contre le diabète de type 2 comme Byetta, approuvés pour la première fois en 2005.
Pour le moment, la FDA se contente « d’évaluer la nécessité d’une action réglementaire ». Il n'a pas encore été demandé aux fabricants de médicaments de prendre des mesures, comme mettre à jour les avertissements figurant sur leurs étiquettes.
Cet examen intervient environ six mois après que l'Agence européenne des médicaments (EMA) a déclaré qu'elle examinerait un lien possible entre les médicaments GLP-1 et les idées suicidaires, après environ 150 rapports sur le sujet.
L'enquête devait initialement se terminer en novembre, mais le comité de l'EMA a récemment soumis « d'autres listes de questions à poser » aux sociétés qui commercialisent des médicaments GLP-1. Le comité devrait réexaminer la question en avril.
De plus, une étude publiée le 5 janvier a examiné une association possible entre le sémaglutide, également connu sous les noms d'Ozempic et Wegovy, et les idées suicidaires. Il a été constaté que ces médicaments ne présentaient pas un risque plus élevé de pensées suicidaires par rapport aux autres médicaments contre le diabète de type 2 et la perte de poids.
Alors que les responsables de la santé et les chercheurs continuent d’explorer les médicaments GLP-1 et tout effet secondaire non répertorié auparavant, les experts conviennent que l’examen ne devrait pas susciter d’inquiétude.
"Je crois que [l'examen est] approprié, c'est leur objectif réglementaire : garantir la sécurité", a déclaré Holly Lofton, MD, directrice du programme médical de gestion du poids de NYU Langone Health.
Bien que le système de déclaration des effets indésirables de la FDA ait identifié une alopécie (chute de cheveux), une aspiration et des idées suicidaires, il ne prouve pas nécessairement que ces effets secondaires ont été causés par les médicaments.
Cependant, le système d'examen FAERS permet à la FDA de surveiller tout problème de sécurité émergent, en particulier lorsqu'un médicament est largement utilisé par le public.
« Ces effets secondaires n’ont pas été observés dans les essais cliniques, mais ceux-ci ne concernent qu’environ 3 000 patients des deux côtés. Sur le marché réel, nous traitons avec des millions de patients », a déclaré Ebne Rafi, PharmD, spécialiste en pharmacie clinique au centre du diabète et de l'obésité des hôpitaux universitaires de Cleveland.
Cet examen représente la FDA « qui remplit son devoir », a-t-il expliqué.
Même s’il n’existe aucun lien confirmé entre les médicaments GLP-1 et les trois effets secondaires identifiés par la FDA, des études antérieures ont suggéré des associations.
Les idées suicidaires sont historiquement associées aux médicaments amaigrissants. Certains médicaments amaigrissants ont même été retirés du marché en raison d'un risque de suicide élevé, a déclaré Lofton. L'impact des médicaments amaigrissants sur le système nerveux central est susceptible de contribuer à ce risque accru, selon Rafi.
Il convient de noter que les idées suicidaires sont répertoriées comme un avertissement dans les informations de prescription de Wegovy.
La perte de cheveux et la perte de poids sont également liées. "L'alopécie est l'un des effets secondaires les plus récents faisant l'objet d'une enquête", a déclaré Rafi. "Une perte de poids rapide pourrait créer des déséquilibres hormonaux et des modifications d'un type particulier de collagène, pouvant entraîner une perte de cheveux dans certains cas."
Cet effet a été observé chez des personnes ayant subi une perte de poids significative après avoir subi une gastrectomie en manchon.
La relation entre les médicaments GLP-1 et l’aspiration pulmonaire (inhalation accidentelle de substances qui aboutissent dans les poumons) est moins claire.
Le Journal canadien d'anesthésie a mis en garde en juillet 2023 contre les patients qui inhalent par inadvertance du contenu gastrique pendant une intervention chirurgicale parce que leur estomac ne peut pas se vider complètement. Il existe peu de recherches sur le lien potentiel entre les médicaments GLP-1 et l'ingestion accidentelle de nourriture dans les voies respiratoires.
Pour l’instant, la FDA se contente « d’évaluer la nécessité d’une action réglementaire », de sorte que les changements futurs dans l’utilisation de ces médicaments, le cas échéant, restent incertains.
Cette action pourrait inclure « la mise à jour des informations sur l’étiquetage d’un produit, la restriction de l’utilisation du médicament, la communication de nouvelles informations sur la sécurité au public ou, dans de rares cas, le retrait d’un produit du marché ».
Cette dernière option est hautement improbable dans le cas des médicaments GLP-1, conviennent les experts. Même s’il existe un lien de causalité entre ces effets secondaires et les médicaments GLP-1, cela ne justifierait pas nécessairement de les rendre indisponibles, a expliqué Rafi.
« Par exemple, les antidépresseurs chimiques présentent le [risque d’idées suicidaires] comme un avertissement majeur. Une majorité de médicaments anti-épileptiques également », a-t-il déclaré. "Et ces médicaments sont sur le marché depuis des années et des années."
Au contraire, la FDA pourrait demander aux entreprises de mettre à jour leurs étiquettes pour inclure ces effets secondaires possibles, ont déclaré les experts. Cela vient de se produire en octobre : la FDA a ajouté un effet secondaire gastro-intestinal, l’iléus, à l’étiquette d’Ozempic.
Quant à la raison pour laquelle ces critiques apparaissent maintenant, Lofton a déclaré que c’est en grande partie à cause de « la grande masse de personnes qui prennent une forme ou une autre de ces médicaments ». En d’autres termes, le nombre d’événements indésirables augmente à mesure que le nombre de personnes prenant ce médicament augmente également.
Bien que l’examen de la FDA soit important, il n’est pas nécessaire que les gens « s’en inquiètent », surtout quand, pour l’instant, il n’y a aucun lien prouvé entre les médicaments GLP-1 et l’alopécie, l’aspiration ou les idées suicidaires, a déclaré Rafi.
Cela est particulièrement vrai pour les personnes qui ont déjà pris le médicament et qui constatent de bons résultats.
" J'ai beaucoup de patients qui viennent et qui prennent ces médicaments depuis des années avec moi, et ils me disent : " Je suis tellement inquiet à propos de l'iléus. " Et je dis : " Eh bien, avez-vous eu un iléus ? " " Non. , je n'ai pas compris.''D'accord, alors ne vous inquiétez pas'', a déclaré Lofton.
Cependant, les patients ou toute personne envisageant de prendre Ozempic, Mounjaro ou un médicament apparenté doivent être conscients de tout risque potentiel et doivent être à l'affût de ces effets secondaires ou d'autres. Cela est d’autant plus vrai que l’expérience de chaque personne en matière de traitement est différente, a-t-elle ajouté.
"En tant que prestataires, nous devons veiller à informer les patients des effets secondaires potentiels, en particulier les plus graves", a déclaré Lofton, "puis assurer un suivi auprès des patients et nous assurer que rien de fâcheux ne les met dans un état où ils courent plus de risques". que d’en tirer profit. »