Können Ozempic und Wegovy Haarausfall und suizidale Ideen verursachen? FDA untersucht Nebenwirkungen von GLP-1-Medikamenten.
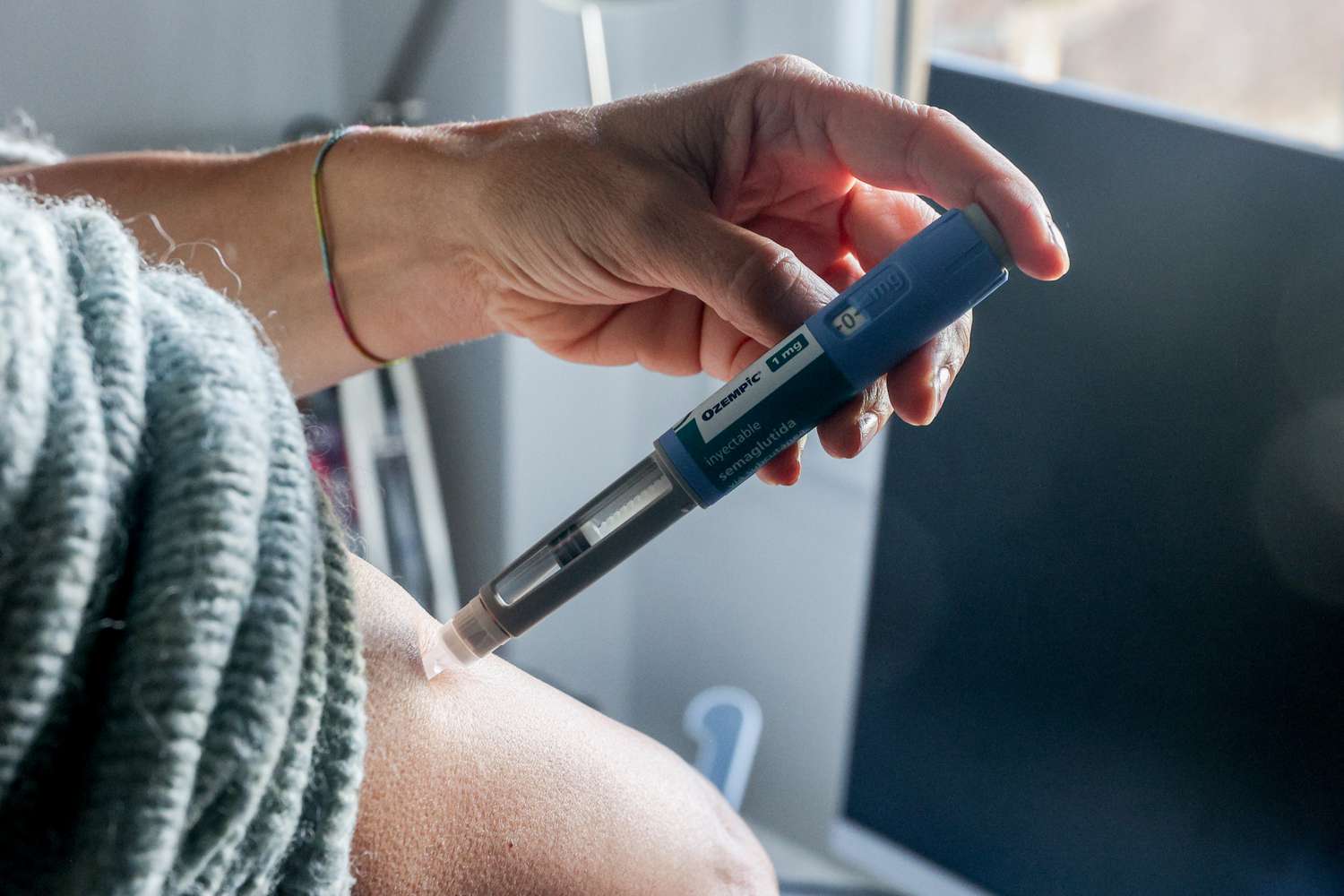
Die Food and Drug Administration (FDA) untersucht derzeit weit verbreitete Medikamente wie Ozempic und Wegovy auf mögliche Zusammenhänge mit Suizidgedanken, Haarausfall und Aspiration.
Berichte über unerwünschte Ereignisse im Zusammenhang mit Glucagon-ähnlichen Peptid-1 (GLP-1)-Rezeptor-Agonisten wurden beim Adverse Event Reporting System (FAERS) der FDA eingereicht. Diese Medikamente sind derzeit Teil einer FDA-Überprüfungsliste, die zuletzt am 2. Januar aktualisiert wurde.
Zu den in Betracht gezogenen GLP-1-Medikamenten gehören neuere wie Wegovy und Mounjaro sowie ältere Typ-2-Diabetes-Medikamente wie Byetta, die erstmals 2005 zugelassen wurden.
Derzeit sei die FDA lediglich dabei, „den Bedarf an regulatorischen Maßnahmen einzuschätzen“. Arzneimittelhersteller wurden bisher nicht aufgefordert, Maßnahmen zu ergreifen, beispielsweise die Warnhinweise auf den Verpackungsetiketten zu aktualisieren.
Diese Untersuchung erfolgt etwa sechs Monate, nachdem die Europäische Arzneimittel-Agentur (EMA) nach etwa 150 Berichten zu diesem Thema erklärt hat, dass sie einen möglichen Zusammenhang zwischen GLP-1-Medikamenten und Selbstmordgedanken prüfen werde.
Ursprünglich wurde erwartet, dass die Untersuchung im November abgeschlossen wird, doch der EMA-Ausschuss hat den Unternehmen, die GLP-1-Medikamente vermarkten, kürzlich „weitere Listen mit zu klärenden Fragen“ vorgelegt. Der Ausschuss wird sich voraussichtlich im April erneut mit dem Thema befassen.
Darüber hinaus untersuchte eine am 5. Januar veröffentlichte Studie einen möglichen Zusammenhang zwischen Semaglutid – auch bekannt als Ozempic und Wegovy – und Selbstmordgedanken. Es wurde festgestellt, dass diese Medikamente im Vergleich zu anderen Medikamenten gegen Typ-2-Diabetes und zur Gewichtsreduktion kein höheres Risiko für Selbstmordgedanken hatten.
Da Gesundheitsbehörden und Forscher weiterhin GLP-1-Medikamente und bisher nicht aufgeführte Nebenwirkungen erforschen, sind sich Experten einig, dass die Überprüfung keinen Grund zur Besorgnis geben sollte.
„Ich glaube, dass [die Überprüfung] angemessen ist, das ist ihr regulatorisches Ziel: Sicherheit zu gewährleisten“, sagte Holly Lofton, MD, Direktorin des medizinischen Gewichtsmanagementprogramms von NYU Langone Health.
Obwohl das unerwünschte Meldesystem der FDA Alopezie (Haarausfall), Aspiration und Selbstmordgedanken identifizierte, beweist es nicht unbedingt, dass diese Nebenwirkungen durch die Medikamente verursacht wurden.
Das FAERS-Überprüfungssystem ermöglicht es der FDA jedoch, alle aufkommenden Sicherheitsprobleme zu überwachen, insbesondere wenn ein Medikament in der Öffentlichkeit weit verbreitet ist.
„Diese Nebenwirkungen wurden in klinischen Studien nicht beobachtet, sie betreffen jedoch nur etwa 3.000 Patienten auf beiden Seiten.“ Auf dem Live-Markt haben wir es mit Millionen von Patienten zu tun“, sagte Ebne Rafi, PharmD, Spezialistin für klinische Pharmazie am Diabetes and Obesity Center der University Hospitals in Cleveland.
Mit dieser Überprüfung erfülle die FDA „ihre Pflicht“, erklärte er.
Auch wenn es keinen bestätigten Zusammenhang zwischen GLP-1-Medikamenten und den drei von der FDA identifizierten Nebenwirkungen gibt, deuten frühere Studien auf Zusammenhänge hin.
Selbstmordgedanken werden seit jeher mit Medikamenten zur Gewichtsreduktion in Verbindung gebracht. Einige Medikamente zur Gewichtsabnahme seien aufgrund eines erhöhten Suizidrisikos sogar vom Markt genommen worden, sagte Lofton. Laut Rafi dürfte die Wirkung von Medikamenten zur Gewichtsreduktion auf das Zentralnervensystem zu diesem erhöhten Risiko beitragen.
Es ist erwähnenswert, dass Suizidgedanken in den Verschreibungsinformationen für Wegovy als Warnung aufgeführt sind.
Haarausfall und Gewichtsverlust hängen ebenfalls zusammen. „Alopezie ist eine der neueren Nebenwirkungen, die untersucht werden“, sagte Rafi. „Schneller Gewichtsverlust kann zu hormonellen Ungleichgewichten und Veränderungen einer bestimmten Art von Kollagen führen, was in manchen Fällen zu Haarausfall führen kann.“
Dieser Effekt wurde bei Personen beobachtet, die nach einer Schlauchmagenoperation einen erheblichen Gewichtsverlust erlitten hatten.
Der Zusammenhang zwischen GLP-1-Medikamenten und Lungenaspiration (versehentliches Einatmen von Stoffen, die in die Lunge gelangen) ist weniger klar.
Das Canadian Journal of Anaesthesia warnte im Juli 2023 davor, dass Patienten während einer Operation versehentlich Mageninhalt einatmen, weil sich ihr Magen nicht vollständig entleeren kann. Es gibt nur begrenzte Forschungsergebnisse zum möglichen Zusammenhang zwischen GLP-1-Medikamenten und der versehentlichen Aufnahme von Nahrungsmitteln in die Atemwege.
Derzeit prüft die FDA nur „die Notwendigkeit regulatorischer Maßnahmen“, so dass die künftigen Änderungen bei der Verwendung dieser Medikamente, falls überhaupt, ungewiss bleiben.
Diese Maßnahme könnte Folgendes umfassen: „Die Aktualisierung der Kennzeichnungsinformationen eines Produkts, die Einschränkung der Verwendung des Arzneimittels, die Übermittlung neuer Sicherheitsinformationen an die Öffentlichkeit oder, in seltenen Fällen, die Entfernung eines Produkts vom Markt.“
Diese letztere Option sei im Fall von GLP-1-Medikamenten höchst unwahrscheinlich, waren sich Experten einig. Auch wenn nachweislich ein kausaler Zusammenhang zwischen diesen Nebenwirkungen und GLP-1-Medikamenten besteht, würde dies nicht unbedingt eine Nichtverfügbarkeit rechtfertigen, erklärte Rafi.
„Zum Beispiel weisen chemische Antidepressiva ein [Suizidgedankenrisiko] als Hauptwarnung auf. Ein Großteil der Medikamente gegen Krampfanfälle auch“, sagte er. „Und diese Medikamente sind schon seit vielen Jahren auf dem Markt.“
Wenn überhaupt, könnte die FDA die Unternehmen auffordern, ihre Etiketten zu aktualisieren, um diese möglichen Nebenwirkungen einzubeziehen, sagten Experten. Dies geschah erst im Oktober – die FDA fügte dem Etikett von Ozempic eine gastrointestinale Nebenwirkung, Ileus, hinzu.
Lofton sagte, dass der Grund, warum diese Rezensionen jetzt auftauchen, vor allem an der „schieren Masse der Menschen liegt, die diese Medikamente in irgendeiner Form einnehmen“. Mit anderen Worten: Die Zahl unerwünschter Ereignisse nimmt zu, da auch die Zahl der Menschen, die das Medikament einnehmen, zunimmt.
Obwohl die FDA-Überprüfung wichtig ist, besteht für die Menschen kein Grund, sich darüber „zu stressen“, insbesondere wenn es derzeit keinen nachgewiesenen Zusammenhang zwischen GLP-1-Medikamenten und Alopezie, Aspiration oder Selbstmordgedanken gibt, sagte Rafi.
Dies gilt insbesondere für Menschen, die die Medikamente bereits eingenommen haben und gute Ergebnisse sehen.
„Ich habe viele Patienten, die zu mir kommen und diese Medikamente seit Jahren mit mir einnehmen, und sie sagen: ‚Ich mache mir solche Sorgen wegen Ileus.‘ Und ich sage: ‚Na, haben Sie Ileus bekommen?‘ ‚Nein „Ich habe es nicht verstanden.“ „Okay, dann mach dir keine Sorgen“, sagte Lofton.
Patienten oder alle, die die Einnahme von Ozempic, Mounjaro oder einem verwandten Arzneimittel in Betracht ziehen, sollten sich jedoch möglicher Risiken bewusst sein und auf diese oder andere Nebenwirkungen achten. Dies gelte insbesondere, da die Erfahrungen jedes Menschen mit dem Medikament anders seien, fügte sie hinzu.
„Als Anbieter müssen wir sicherstellen, dass die Patienten auf mögliche Nebenwirkungen aufmerksam gemacht werden, insbesondere auf die schwerwiegenden“, sagte Lofton, „und dann mit den Patienten weitermachen und sicherstellen, dass nichts Ungewöhnliches sie in einen Zustand versetzt, in dem sie einem höheren Risiko ausgesetzt sind.“ als Nutzen.“




