Banbrytare inom Genetik: Forskare Jakar på Kuren för Sällsynta Ärftliga Sjukdomar
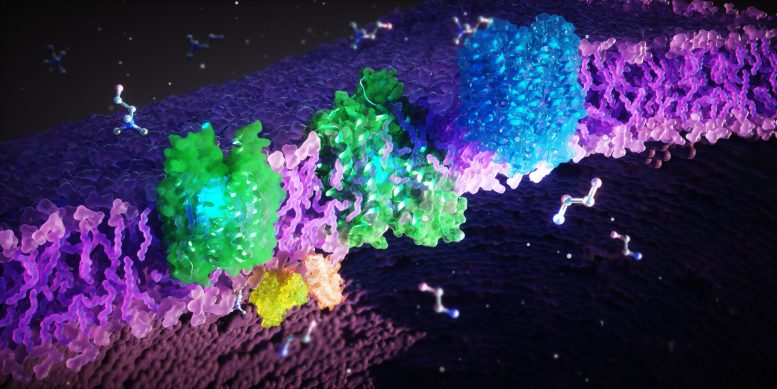
Ett internationellt team har identifierat strukturerna och de avgörande funktionerna hos FLVCR1 och FLVCR2 proteiner, som transporterar huvudmolekyler som påverkar cellulär hälsa. Denna forskning ökar förståelsen för sällsynta genetiska sjukdomar kopplade till dessa proteiner och öppnar upp vägar för utveckling av nya behandlingsformer. FLVCR-proteinerna (gröna, blåa) sitter i cellmembranet (lila). Dessa proteiner transporterar de cellbyggande klossarna etanolamin och kolin över membranet. Kredit: Ella Maru Studio
Det är känt att brister i dessa proteiner FLVCR1 och FLVCR2 leder till sällsynta ärftliga sjukdomar hos människor som orsakar motoriska, sensoriska och neurologiska störningar. Bio-kemiska mekanismer bakom detta och de fysiologiska funktionerna hos FLVCR-proteinerna har tidigare varit oklara.
Ett tvärvetenskapligt team av forskare från Frankfurt am Main, Singapore och USA har nu kartlagt FLVCR-proteinernas 3D-strukturer och deras cellulära funktioner. Forskarna har visat att proteinerna transporterar de cellbyggande klossarna kolin och etanolamin, vilket bidrar till förståelsen för uppkomsten av sällsynta sjukdomar och utvecklingen av nya behandlingsmetoder.
I sjukhus-tv-serier som Scrubs eller Dr. House söker läkare efter rätt diagnoser och möjliga behandlingar för patienter med ibland förbryllande eller konstiga symptom. I verkligheten tar denna process ofta år för de som drabbats av sällsynta sjukdomar. I många fall finns det ingen effektiv medicin och terapeutiska alternativ är begränsade.
Ungefär 6-8% av världens befolkning lider av en sällsynt sjukdom. Det innebär närmare 500 miljoner människor, trots att var och en av de över 7000 olika sjukdomarna bara drabbar ungefär en av 2000 människor. Eftersom dessa sjukdomar är så sällsynta, är medicinsk och vetenskaplig kunskap om dem begränsade. Det finns bara ett fåtal experter världen över och det sociala medvetandet är lågt.
Ett internationellt forskarteam leddes av Schara Safarian, projektgruppsledare vid Max Planck Institute of Biophysics samt oberoende gruppchef vid Fraunhofer Institute for Translational Medicine and Pharmacology ITMP och Institute of Clinical Pharmacology vid Goethe-Universität Frankfurt, har nu undersökt strukturen och den cellulära funktionen av två proteiner, FLVCR1 och FLVCR2, vilka spelar en orsakande roll i ett antal sällsynta ärftliga sjukdomar. Forskarna har publicerat sina rön i den prestigefyllda tidskriften Nature.
Felaktigheter av FLVCR1 och FLVCR2 på grund av genmutationer orsakar sällsynta sjukdomar, varav vissa leder till svåra syn-, rörelse- och sensoriska störningar - som "posterior column ataxia with retinitis pigmentosa", "Fowler’s syndrome" eller sensoriska och autonoma neuropatier. Dessa kan exempelvis leda till fullständig förlust av smärtupplevelse. "I många sjukdomar, inklusive de sällsynta, förändras cellulära strukturer i vår kropp och detta leder till funktionsfel i biokemiska processer", säger Schara Safarian. "För att förstå utvecklingen av sådana sjukdomar och utveckla behandlingar, behöver vi veta hur dessa proteiner är strukturerade på molekylär nivå och vilka funktioner de utför i friska celler."
Forskarna har upptäckt att FLVCR 1 och FLVCR2 transporterar molekylerna cholin och etanolamin över membranen i våra celler. "Kolin och etanolamin är nödvändiga för viktiga kroppsfunktioner. De stöder tillväxt, regenerering och stabilitet i våra celler, till exempel i muskler, inre organ och hjärnan", förklarar Safarian. "Dessutom är kolin inblandad i fettmetabolism och avgiftning av levern. Vår kropp behöver också det för att producera neurotransmittorn acetylkolin som är avgörande för vårt nervsystem och behövs av vår hjärna för att kontrollera organen. Så man kan föreställa sig att fel på FLVCR-proteiner kan orsaka allvarliga neurologiska och muskulösa störningar."
Forskarna använde mikroskopiska, biokemiska och datorassisterade metoder för att undersöka FLVCR-proteinerna. "Vi skrämsel-frös proteinerna och observerade dem sedan i ett elektronmikroskop", förklarar Di Wu, forskare vid Max Planck Institute of Biophysics och medförfattare till studien. "En elektronstråle tränger igenom det frysta provet och interaktionen av elektronerna med materialet skapar en bild". Forskarna tar många individuella bilder och bearbetar dem och kombinerar dem beräkningsmässigt för att få högupplösta 3D-strukturer av proteiner. På detta sätt kunde de avkoda strukturerna för FLVCR1 och FLVCR2 och se hur de förändras i närvaro av etanolamin och kolin. Datorsimuleringar bekräftade och visualiserade hur FLVCR-proteinerna interagerar med etanolamin och kolin, och dynamiskt ändrar sin struktur för att möjliggöra näringsämnen transport.
Safarian summarizes: “Our findings pave the way for understanding the development and progression of rare diseases associated with the FLVCR proteins. In the future, patients may be able to benefit from new therapies that restore their life quality.”
Reference: “Molecular mechanism of choline and ethanolamine transport in humans” by Keiken Ri, Tsai-Hsuan Weng, Ainara Claveras Cabezudo, Wiebke Jösting, Yu Zhang, Andre Bazzone, Nancy C. P. Leong, Sonja Welsch, Raymond T. Doty, Gonca Gursu, Tiffany Jia Ying Lim, Sarah Luise Schmidt, Janis L. Abkowitz, Gerhard Hummer, Di Wu, Long N. Nguyen and Schara Safarian, 22 May 2024, Nature. DOI: 10.1038/s41586-024-07444-7