Frühe mRNA-Forschung, die zu COVID-19-Impfstoffen führte, gewinnt den Nobelpreis für Medizin 2023.
Zwei Wissenschaftler, die die Grundlage für das gelegt haben, was zu den einflussreichsten Impfstoffen aller Zeiten werden würde, erhielten den Nobelpreis 2023 in Medizin oder Physiologie.
Die Biochemikerin Katalin Karikó, jetzt an der Universität Szeged in Ungarn, und Drew Weissman von der University of Pennsylvania wurden für ihre Forschung über Modifikationen von mRNA ausgezeichnet, die die ersten Impfstoffe gegen COVID-19 ermöglichten.
"Jeder hat die COVID-19-Pandemie erlebt, die unser Leben, unsere Wirtschaft und unsere öffentliche Gesundheit beeinflusst. Es war ein traumatisches Ereignis", sagte Qiang Pan-Hammarström, Mitglied der Nobelversammlung am Karolinska-Institut in Stockholm, das den Medizin- oder Physiologiepreis vergibt. Ihre Äußerungen erfolgten am 2. Oktober nach einer Pressekonferenz zur Bekanntgabe der Gewinner. "Sie müssen wahrscheinlich nicht weiter betonen, dass die grundlegende Entdeckung der Laureaten einen enormen Einfluss auf unsere Gesellschaft hat."
Bis September 2023 wurden laut Weltgesundheitsorganisation mehr als 13,5 Milliarden COVID-19-Impfstoffdosen - einschließlich mRNA-Impfstoffen sowie anderen Arten von Impfungen - verabreicht, seit diese erstmals im Dezember 2020 verfügbar wurden. Im Jahr nach ihrer Einführung haben die Impfungen weltweit schätzungsweise fast 20 Millionen Menschenleben gerettet. In den Vereinigten Staaten, wo mRNA-Impfungen gegen COVID-19 von Moderna und Pfizer/BioNTech den Großteil der Impfungen ausmachten, wird geschätzt, dass die Impfstoffe 1,1 Millionen zusätzliche Todesfälle und 10,3 Millionen Krankenhausaufenthalte verhindert haben.
RNA ist der weniger bekannte chemische Cousin von DNA. Zellen stellen RNA-Kopien der genetischen Anweisungen her, die in DNA enthalten sind. Einige dieser RNA-Kopien, bekannt als Messenger-RNA oder mRNA, werden verwendet, um Proteine aufzubauen. Messenger-RNA "sagt Ihren Zellen buchstäblich, welche Proteine hergestellt werden sollen", sagt Kizzmekia Corbett-Helaire, eine virale Immunologin an der Harvard T. H. Chan School of Public Health in Boston. Proteine erledigen einen Großteil der wichtigen Arbeiten, die Zellen und die Organismen, zu denen sie gehören, am Leben und gesund erhalten.
Die mRNA-Impfstoffe funktionieren etwas anders als herkömmliche Impfungen. Die meisten traditionellen Impfstoffe verwenden Viren oder Bakterien - entweder abgeschwächt oder abgetötet - oder Proteine von diesen Erregern, um das Immunsystem dazu zu bringen, schützende Antikörper und andere Abwehrkräfte gegen zukünftige Infektionen zu bilden.
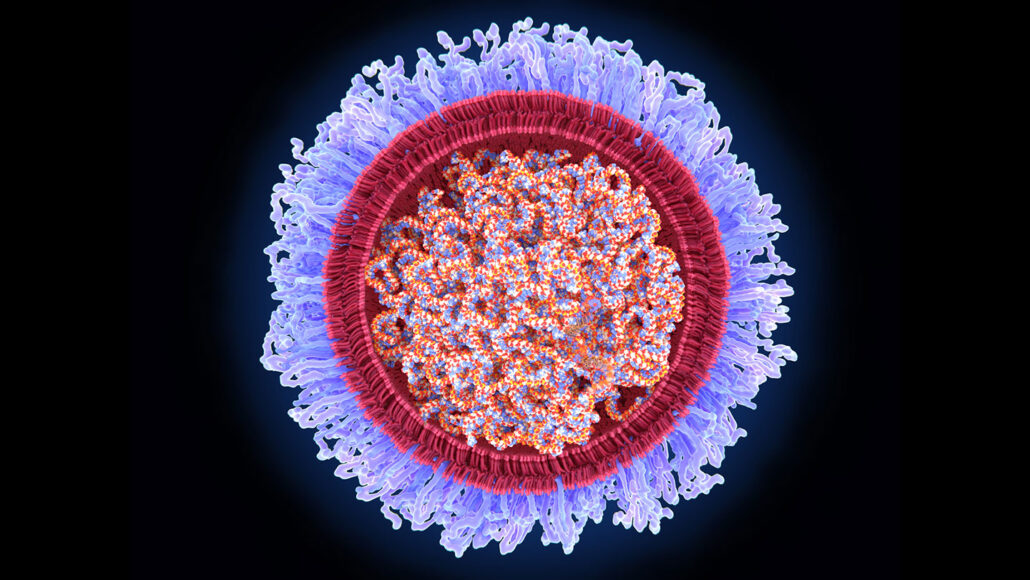
Die COVID-19-Impfstoffe von Pfizer/BioNTech und Moderna enthalten stattdessen mRNA, die Anweisungen zur Herstellung eines der Proteine des Coronavirus enthält. Wenn eine Person eine mRNA-Impfung erhält, gelangt das genetische Material in ihre Zellen und löst die Produktion des viralen Proteins für eine kurze Zeit aus. Wenn das Immunsystem das virale Protein erkennt, baut es Abwehrmechanismen auf, um bei einer späteren Infektion mit dem Coronavirus schwere Erkrankungen zu verhindern.
Messenger-RNA-Impfstoffe waren eine gute Wahl, um die Pandemie zu bekämpfen, sagt Corbett-Helaire. Die Technologie ermöglicht es Wissenschaftlern, "diesen Schritt der Herstellung großer Mengen von Proteinen im Labor zu überspringen und stattdessen dem Körper beizubringen, Dinge zu tun, die der Körper bereits tut, außer dass wir jetzt ein zusätzliches Protein herstellen", sagt sie.
Abgesehen von ihrem Schutz vor dem Coronavirus könnten mRNA-Impfstoffe auch gegen andere Infektionskrankheiten und Krebs wirksam sein. Wissenschaftler könnten die Technologie auch nutzen, um Menschen mit bestimmten seltenen genetischen Erkrankungen dabei zu helfen, Enzyme oder andere Proteine zu produzieren, die ihnen fehlen. Klinische Studien zu vielen dieser Anwendungen sind im Gange, aber es könnte Jahre dauern, bevor Wissenschaftler die Ergebnisse kennen.
Der erste mRNA-Impfstoff gegen COVID-19 wurde knapp ein Jahr nach Beginn der Pandemie verfügbar, aber die dahinterstehende Technologie wurde über Jahrzehnte entwickelt.
Bekommen Sie exzellenten Wissenschaftsjournalismus von der vertrauenswürdigsten Quelle direkt an Ihre Haustür.
1997 trafen Karikó und Weissman sich an der Kopiermaschine, sagte Karikó während einer Pressekonferenz am 2. Oktober an der University of Pennsylvania. Sie erzählte ihm von ihrer Arbeit mit RNA und er teilte sein Interesse an Impfstoffen. Obwohl sie in verschiedenen Gebäuden untergebracht waren, arbeiteten die Forscher zusammen, um ein grundlegendes Problem zu lösen, das mRNA-Impfstoffe und Therapien hätte scheitern lassen können: Die Injektion von unveränderter mRNA in den Körper sorgt auf schlechte Weise dafür, dass das Immunsystem aktiviert wird und eine Flut von immunkritischen Chemikalien namens Zytokine produziert. Diese Chemikalien können schädliche Entzündungen auslösen. Und diese unveränderte mRNA produziert im Körper sehr wenig Protein.
Die Forscher fanden heraus, dass der Austausch des RNA-Bausteins Uracil gegen modifizierte Versionen, zuerst Pseudouridin und dann N1-Methylpseudouridin, die schlechte Immunreaktion schwächen konnte. Diese raffinierte Chemie, erstmals 2005 berichtet, ermöglichte es den Forschern, die Immunreaktion einzudämmen und die mRNA sicher in die Zellen zu transportieren.
“The messenger RNA has to hide and it has to go unnoticed by our bodies, which are very brilliant at destroying things that are foreign,” Corbett-Helaire says. “The modifications that [Karikó and Weissman] worked on for a number of years really were fundamental to allowing the mRNA therapeutics to hide while also being very helpful to the body.”
In addition, the modified mRNA produced lots of protein that could spark an immune response, the team showed in 2008 and 2010. It was this work on modifying mRNA building blocks that the prize honors.
For years, “we couldn’t get people to notice RNA as something interesting,” Weissman said at the Penn news conference. Vaccines using the technology failed clinical trials in the early 1990s, and most researchers gave up. But Karikó “lit the match,” and they spent the next 20 years figuring out how to get it to work, Weissman said. “We would sit together in 1997 and afterwards and talk about all the things that we thought RNA could do, all of the vaccines and therapeutics and gene therapies, and just realizing how important it had the potential to be. That’s why we never gave up.”
In 2006, Karikó and Weissman started a company called RNARx to develop mRNA-based treatments and vaccines. After Karikó joined the German company BioNTech in 2013, she and Weissman continued to collaborate. They and colleagues reported in 2015 that encasing mRNA in bubbles of lipids could help the fragile RNA get into cells without getting broken down in the body. The researchers were developing a Zika vaccine when the pandemic hit, and quickly applied what they had learned toward containing the coronavirus.
The duo’s work was not always so celebrated. Thomas Perlmann, Secretary General of the Nobel Assembly at the Karolinska Institute, asked the newly minted laureates whether they were surprised to have won. He said that Karikó was overwhelmed, noting that just 10 years ago she was terminated from her job and had to move to Germany without her family to get another position. She never won a grant from the U.S. National Institutes of Health to support her work.
“She struggled and didn’t get recognition for the importance of her vision,” Perlmann said, but she had a passion for using mRNA therapeutically. “She resisted the temptation to sort of go away from that path and do something maybe easier.” Karikó is the 61st woman to win a Nobel Prize since 1901, and the 13th to be awarded a prize in physiology and medicine.
Though it often takes decades before the Nobel committees recognize a discovery, sometimes recognition comes relatively swiftly. For instance, Emmanuelle Charpentier and Jennifer Doudna won the Nobel Prize for chemistry in 2020 a mere eight years after the researchers published a description of the genetic scissors CRISPR/Cas 9 (SN: 10/7/20).
“I never expected in my entire life to get the Nobel Prize,” Weissman said, especially not a mere three years after the vaccines demonstrated their medical importance. Perlmann told him the Nobel committee was seeking to be “more current” with its awards, he said.
The timely Nobel highlights that “there are just a million other possibilities for messenger RNA therapeutics … beyond the vaccines,” Corbett-Helaire says.
The researchers said at the Penn news conference that they weren’t sure the early morning phone call from Perlmann was real. On the advice of Weissman’s daughter, they waited for the Nobel announcement. “We sat in bed. [I was] looking at my wife, and my cat is begging for food,” he said. “We wait, and the press conference starts, and it was real. So that’s when we really became excited.”
Karikó and Weissman will share the prize of 11 million Swedish kronor, or roughly $1 million.
Our mission is to provide accurate, engaging news of science to the public. That mission has never been more important than it is today.
As a nonprofit news organization, we cannot do it without you.
Your support enables us to keep our content free and accessible to the next generation of scientists and engineers. Invest in quality science journalism by donating today.




