Les premières recherches sur les ARNm qui ont conduit aux vaccins contre le COVID-19 remportent le prix Nobel de médecine 2023.
Deux scientifiques qui ont posé les bases de ce qui deviendrait parmi les vaccins les plus influents de tous les temps ont été récompensés par le prix Nobel de médecine ou de physiologie 2023.
La biochimiste Katalin Karikó, actuellement à l'Université de Szeged en Hongrie, et Drew Weissman de l'Université de Pennsylvanie ont été honorés pour leurs recherches sur les modifications de l'ARNm qui ont rendu possibles les premiers vaccins contre la COVID-19 (SN: 12/15/21).
"Tout le monde a vécu la pandémie de COVID-19 qui affecte notre vie, notre économie et notre santé publique. C'était un événement traumatisant", a déclaré Qiang Pan-Hammarström, membre de l'Assemblée Nobel à l'Institut Karolinska de Stockholm, qui décerne le prix de médecine ou de physiologie. Ses remarques ont été faites le 2 octobre lors d'un point presse pour annoncer les lauréats. "Vous n'avez probablement pas besoin d'insister davantage sur le fait que la découverte fondamentale faite par les lauréats a eu un énorme impact sur notre société."
En septembre 2023, plus de 13,5 milliards de doses de vaccins contre la COVID-19, y compris des vaccins à ARNm ainsi que d'autres types de vaccins, avaient été administrées depuis leur première disponibilité en décembre 2020, selon l'Organisation mondiale de la santé. Au cours de l'année suivant leur introduction, on estime que ces vaccins ont sauvé près de 20 millions de vies dans le monde entier. Aux États-Unis, où les vaccins à ARNm contre la COVID-19 fabriqués par Moderna et Pfizer/BioNTech représentaient la grande majorité des vaccinations, on estime que les vaccins ont permis d'éviter 1,1 million de décès supplémentaires et 10,3 millions d'hospitalisations.
L'ARN est le cousin chimique moins connu de l'ADN. Les cellules fabriquent des copies d'ARN des instructions génétiques contenues dans l'ADN. Certaines de ces copies d'ARN, appelées ARN messager, ou ARNm, sont utilisées pour construire des protéines. L'ARNm "dit littéralement à vos cellules quelles protéines fabriquer", déclare Kizzmekia Corbett-Helaire, immunologiste viral à la Harvard T. H. Chan School of Public Health de Boston. Les protéines effectuent une grande partie du travail important qui maintient les cellules, et les organismes dont elles font partie, en vie et en bonne santé.
Les vaccins à ARNm fonctionnent un peu différemment des immunisations traditionnelles. La plupart des vaccins traditionnels utilisent des virus ou des bactéries - soit affaiblis, soit tués - ou des protéines provenant de ces agents pathogènes pour provoquer une réponse immunitaire et produire des anticorps protecteurs ainsi que d'autres défenses contre les futures infections.
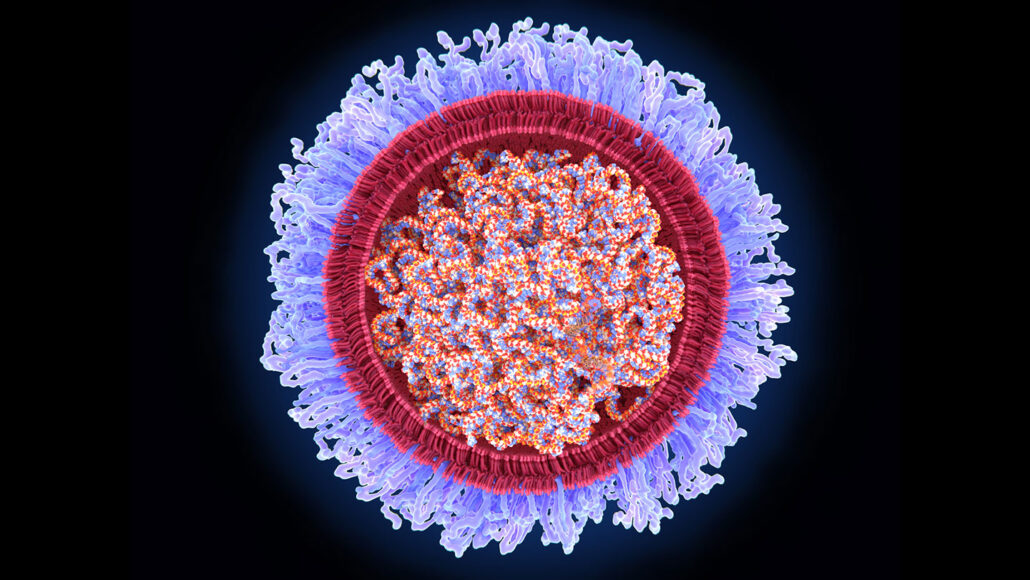
Les vaccins COVID-19 fabriqués par Pfizer/BioNTech et Moderna contiennent plutôt de l'ARNm qui contient les instructions pour fabriquer l'une des protéines du coronavirus (SN: 2/21/20). Lorsqu'une personne reçoit une injection d'ARNm, le matériel génétique pénètre dans ses cellules et incite les cellules à produire la protéine virale pendant une courte période. Lorsque le système immunitaire voit la protéine virale, il met en place des défenses pour prévenir une maladie grave si la personne est ultérieurement infectée par le coronavirus.
Les vaccins utilisant l'ARNm étaient un bon choix pour lutter contre la pandémie, explique Corbett-Helaire. La technologie permet aux scientifiques de "sauter cette étape de production de grandes quantités de protéines en laboratoire et, à la place... de dire au corps de faire ce que le corps fait déjà, à l'exception que nous fabriquons une protéine supplémentaire", dit-elle.
En plus de protéger les personnes contre le coronavirus, les vaccins à ARNm pourraient également être efficaces contre d'autres maladies infectieuses et le cancer. Les scientifiques pourraient également utiliser la technologie pour aider les personnes atteintes de certaines maladies génétiques rares à produire des enzymes ou d'autres protéines qui leur font défaut. Des essais cliniques sont en cours pour plusieurs de ces utilisations, mais il faudra peut-être des années avant que les scientifiques connaissent les résultats (SN: 12/17/21).
Le premier vaccin à ARNm contre la COVID-19 est devenu disponible juste avant un an de pandémie, mais la technologie qui le sous-tend est en développement depuis des décennies.
Obtenez un excellent journalisme scientifique, provenant de la source la plus fiable, livré à votre porte.
En 1997, Karikó et Weissman se sont rencontrés à la photocopieuse, a déclaré Karikó lors d'une conférence de presse le 2 octobre à l'Université de Pennsylvanie. Elle lui a parlé de son travail avec l'ARN, et il a partagé son intérêt pour les vaccins. Bien qu'ils se trouvent dans des bâtiments séparés, les chercheurs ont travaillé ensemble pour résoudre un problème fondamental qui aurait pu compromettre les vaccins et thérapies à ARNm : l'injection d'ARNm classique dans le corps provoque une réaction immunitaire néfaste, produisant un afflux de produits chimiques immunitaires appelés cytokines. Ces produits chimiques peuvent déclencher une inflammation dommageable. De plus, cet ARNm non modifié produit très peu de protéines dans le corps.
Les chercheurs ont découvert que le remplacement du nucléotide uridine par des versions modifiées, d'abord la pseudouridine puis la N1-méthylpseudouridine, pouvait atténuer la mauvaise réaction immunitaire. Cette chimie astucieuse, rapportée pour la première fois en 2005, a permis aux chercheurs de maîtriser la réponse immunitaire et de délivrer en toute sécurité l'ARNm aux cellules.
“The messenger RNA has to hide and it has to go unnoticed by our bodies, which are very brilliant at destroying things that are foreign,” Corbett-Helaire says. “The modifications that [Karikó and Weissman] worked on for a number of years really were fundamental to allowing the mRNA therapeutics to hide while also being very helpful to the body.”
In addition, the modified mRNA produced lots of protein that could spark an immune response, the team showed in 2008 and 2010. It was this work on modifying mRNA building blocks that the prize honors.
For years, “we couldn’t get people to notice RNA as something interesting,” Weissman said at the Penn news conference. Vaccines using the technology failed clinical trials in the early 1990s, and most researchers gave up. But Karikó “lit the match,” and they spent the next 20 years figuring out how to get it to work, Weissman said. “We would sit together in 1997 and afterwards and talk about all the things that we thought RNA could do, all of the vaccines and therapeutics and gene therapies, and just realizing how important it had the potential to be. That’s why we never gave up.”
In 2006, Karikó and Weissman started a company called RNARx to develop mRNA-based treatments and vaccines. After Karikó joined the German company BioNTech in 2013, she and Weissman continued to collaborate. They and colleagues reported in 2015 that encasing mRNA in bubbles of lipids could help the fragile RNA get into cells without getting broken down in the body. The researchers were developing a Zika vaccine when the pandemic hit, and quickly applied what they had learned toward containing the coronavirus.
The duo’s work was not always so celebrated. Thomas Perlmann, Secretary General of the Nobel Assembly at the Karolinska Institute, asked the newly minted laureates whether they were surprised to have won. He said that Karikó was overwhelmed, noting that just 10 years ago she was terminated from her job and had to move to Germany without her family to get another position. She never won a grant from the U.S. National Institutes of Health to support her work.
“She struggled and didn’t get recognition for the importance of her vision,” Perlmann said, but she had a passion for using mRNA therapeutically. “She resisted the temptation to sort of go away from that path and do something maybe easier.” Karikó is the 61st woman to win a Nobel Prize since 1901, and the 13th to be awarded a prize in physiology and medicine.
Though it often takes decades before the Nobel committees recognize a discovery, sometimes recognition comes relatively swiftly. For instance, Emmanuelle Charpentier and Jennifer Doudna won the Nobel Prize for chemistry in 2020 a mere eight years after the researchers published a description of the genetic scissors CRISPR/Cas 9 (SN: 10/7/20).
“I never expected in my entire life to get the Nobel Prize,” Weissman said, especially not a mere three years after the vaccines demonstrated their medical importance. Perlmann told him the Nobel committee was seeking to be “more current” with its awards, he said.
The timely Nobel highlights that “there are just a million other possibilities for messenger RNA therapeutics … beyond the vaccines,” Corbett-Helaire says.
The researchers said at the Penn news conference that they weren’t sure the early morning phone call from Perlmann was real. On the advice of Weissman’s daughter, they waited for the Nobel announcement. “We sat in bed. [I was] looking at my wife, and my cat is begging for food,” he said. “We wait, and the press conference starts, and it was real. So that’s when we really became excited.”
Karikó and Weissman will share the prize of 11 million Swedish kronor, or roughly $1 million.
Our mission is to provide accurate, engaging news of science to the public. That mission has never been more important than it is today.
As a nonprofit news organization, we cannot do it without you.
Your support enables us to keep our content free and accessible to the next generation of scientists and engineers. Invest in quality science journalism by donating today.




