Ein DNA-Montage-Set, um das Potenzial von CRISPR-Cas9 für Stoffwechseltechnik freizusetzen.
30. August 2023 Merkmale
Dieser Artikel wurde gemäß dem redaktionellen Prozess und den Richtlinien von Science X überprüft. Die Redakteure haben folgende Merkmale hervorgehoben, um die Glaubwürdigkeit des Inhalts sicherzustellen:
- Tatsachenprüfung
- Peer-Review-Publikation
- vertrauenswürdige Quelle
- korrekturgelesen
von Thamarasee Jeewandara, Phys.org
Die clustered regularly interspaced short palindrome repeats (CRISPR) und das Crispr-assoziierte Protein 9 (CRISPR/Cas9) sind heute eine bekannte, revolutionäre Methode zur Veränderung von mikrobiellen Zellen.
Ein wesentlicher Vorteil von CRISPR besteht darin, dass es das Stammesdesign erleichtert, um die chromosomale Integration zur Montage von markerfreier DNA zu ermöglichen. Diese Bearbeitungssysteme sind sehr vorteilhaft, aber ihre Montage ist nicht ganz einfach und kann die Verwendung und Anwendungen verhindern.
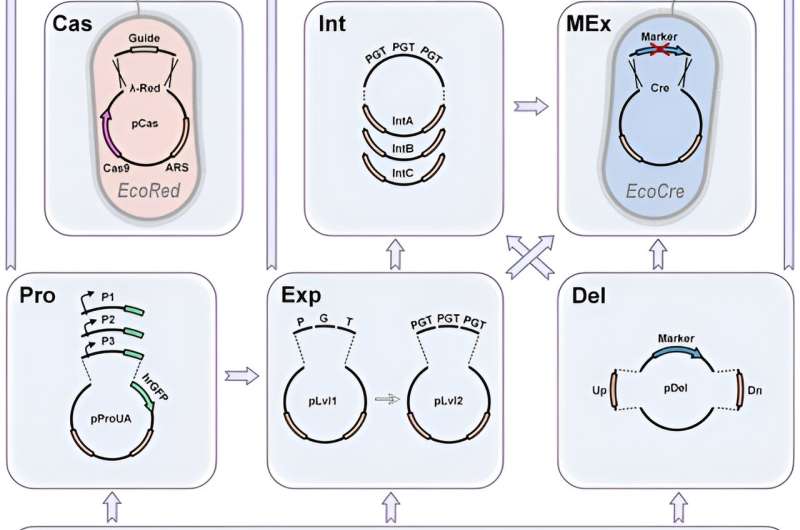
In einem neuen Bericht in Nature Communications Biology identifizierten Tigran V. Yuzbashev und ein Forschungsteam die Grenzen der bestehenden Cas9-Toolkits, die entwickelt wurden, um den Zugang zu CRISPR-Techniken zu erleichtern und zu implementieren. Sie diskutierten drei verschiedene etablierte Methoden und kombinierten sie zu einem umfassenden Toolkit für effiziente Stoffwechseltechnik mit Hilfe von CRISPR/Cas9.
Ein einziges Toolkit bestehend aus 147 Plasmiden wurde verwendet, um eine Bibliothek von 137 Promotoren zur Herstellung von Homogentisinsäure im Labor zu generieren und zu charakterisieren.
Das CRISPR/Cas9-System ermöglicht schnelle, präzise und narbenfreie genomische Modifikationen und bietet damit große Möglichkeiten zur Gestaltung von mikrobiellen Stämmen für die Bioproduktion. Die metabolische Ingenieurskunst von Hefen beispielsweise ist ein schnell wachsendes Gebiet der Biotechnologie zur nachhaltigen Produktion von Chemikalien, Kraftstoffen, Lebensmitteln und Arzneimitteln.
Hefen haben ein ähnliches Stoffwechselpotential wie eukaryotische Zellen und lassen sich daher leichter verändern und im großen Maßstab kultivieren. Aus diesem Grund haben Bioingenieure CRISPR-Systeme für Hefen entwickelt.
Aufgrund seiner hohen Effizienz ermöglicht CRISPR markerlose genomische Modifikationen. In dieser Arbeit optimierte Yuzbashev den Stamm und erleichterte metabolische Ingenieursprojekte, indem er drei Verbesserungen des CRISPR/Cas9-Systems für die Hefen-Technik identifizierte. Die Methoden umfassten: 1) den einfachen Austausch zwischen Marker- und markerloser Modifikation, 2) den schnellen Austausch von Homologieschenkeln zur Bestimmung verschiedener Integrationsorte und 3) eine einfache Methode zum Klonen von gRNAs.
Um eine markerfreie Integration auf der Grundlage von CRISPR zu ermöglichen, wählte das Team einen Doppelstrangbruch aus, der durch Cas9 verursacht wurde und zur Vermehrung der Zellen repariert werden musste. Die Wissenschaftler machten dies möglich, indem sie eine Vorlage oder einen Spender verwendeten, der durch homologe Rekombination oder nicht-homologes Endverbinden (NHEJ) integriert wurde - ohne Integration. Der Prozess der nicht-homologen Endverbinden wird bei den meisten pilzlichen Arten beobachtet, einschließlich der Backhefe Saccharomyces cerevisiae.
Bei Arten mit einem vorherrschenden NHEJ-Mechanismus verbesserte das Team die homologe Rekombination, indem sie die NHEJ-Gene löschte. Wenn eine markerfreie Methode nicht erfolgreich war, beabsichtigten die Wissenschaftler anschließend, die CRISPR-Cas9-unterstützte Integration zur leichteren Rückkehr zur markerbasierten Integration zu verbessern.
Die Cas9-unterstützte Integration erfordert in der Regel eine Spender-Vorlage, bestehend aus einem integrierten Kassetten-Flanking von zwei Homologieschenkeln. Das Team postulierte, dass die ideale Integration von CRISPR-Cas9 Homologieschenkel auf vorab bewerteten Cas9-Spenderkonstrukten über eine vereinfachte Golden Gate Assembly-Reaktion austauschen sollte.
Promotoren sind zudem ein Schlüsselelement für jedes metabolische Ingenieursprojekt, um den Fluss in Richtung der gewünschten Produkte umzuleiten. Yuzbashev et al. verwendeten die industrielle Hefe Yarrowia lipolytica, um ein metabolisches Ingenieurswerkzeug zu entwickeln, das Genomeditierung und DNA-Montagestrategien für hohe Effizienz und Vielseitigkeit kombiniert.
Die Wissenschaftler erschlossen das volle Potenzial von CRISPR/Cas9 für die metabolische Ingenieurskunst, indem sie ein Toolkit entwickelten, das auf zuvor bekannten Golden Gate Assembly-Systemen aufbaute. Sie testeten das Screening-System, indem sie mehrere Promotorbibliotheken erzeugten. Yuzbashev et al. wählten Y. lipolytica ribosomale Gene aus, die Proteine der großen und kleinen Untereinheiten kodieren. Sie identifizierten eine Vielzahl von Promotoren mit unterschiedlichen Stärken, um die Anzahl der Promotoren für dasselbe Organismus zu erweitern.
Um den Einfluss und die Verwendung der verbesserten CRISPR/Cas9-Methode zu beweisen, entwickelte das Team eine Y. lipolytica durch rationale Ingenieurskunst, um Homogentisinsäure (HGA) zu produzieren. Typischerweise oxidiert HGA unter alkalischen Bedingungen spontan zu selbstpolymerisiertem Pyomelanin - ein hervorragender Bestandteil von natürlichen Sonnenschutzmitteln und Kosmetika.
Despite its high commercial potential, existing methods to produce the acid precursor and pyomelanin product relied on the biotransformation of expensive aromatic amino acids. To facilitate metabolic engineering, the team therefore first selected several genes that encoded theprecursor aromatic aminotransferases as engineering targets. They then selected three overexpression targets to enhance the de novo synthesis of the homogentisic acid in the model organism. Finally, they studied and inactivated the HGA degradation pathway; a path yet unknown to exist in Y. lipolytica.
In this way, Tigran V. Yuzbashev and colleagues showed the dependence of metabolic engineering of living organisms on efficient DNA manipulation methods. This work presents an example of an enhanced molecular toolkit designed for CRISPR/Cas9-based metabolic engineering.
The scientists proved the functionality of the platform for both rapid strain construction and the characterization of a large library of promoters. They anticipate for this toolkit to have broader applications in strain engineering and in industry. The team envision for the Y. lipolytica model developed in this work to have overarching applications in other fields of biological engineering as well.
Guri Giaever et al, Functional profiling of the Saccharomyces cerevisiae genome, Nature (2002). DOI: 10.1038/nature00935
Journal information: Nature , Communications Biology
© 2023 Science X Network




