Un kit de ensamblaje de ADN para desbloquear el potencial de CRISPR-Cas9 en ingeniería metabólica.
30 de agosto de 2023
Característica
Este artículo ha sido revisado de acuerdo con el proceso editorial y las políticas de Science X. Los editores han destacado las siguientes características al asegurar la credibilidad del contenido:
- verificado por hechos
- publicación revisada por pares
- fuente confiable
- corregido de errores
por Thamarasee Jeewandara, Phys.org
El sistema CRISPR (repetición palindrómica corta agrupada y regularmente interespaciada) y la proteína asociada a CRISPR 9 (CRISPR/Cas9) es ahora un método revolucionario bien conocido para modificar células microbianas.
Una ventaja clave de CRISPR radica en el diseño de la cepa para facilitar la integración cromosómica y permitir la construcción de ADN sin marcadores. Estos sistemas de edición son muy beneficiosos; sin embargo, su ensamblaje no es tan sencillo y puede evitar su uso y aplicaciones.
En un nuevo informe en Nature Communications Biology, Tigran V. Yuzbashev y un equipo de investigación identificaron los límites de los kits de herramientas existentes de Cas9 diseñados para facilitar el acceso e implementación de las técnicas de CRISPR. Discutieron tres métodos diferentes bien establecidos y los combinaron para formar un kit de herramientas integral para la ingeniería metabólica eficiente mediante el uso de CRISPR/Cas9.
Un solo kit de herramientas comprende 147 plásmidos para generar y caracterizar una biblioteca de 137 promotores para construir ácido homogentísico en el laboratorio.
El sistema CRISPR/Cas9 puede realizar modificaciones genómicas rápidas, precisas y sin cicatrices para proporcionar un amplio campo para diseñar cepas microbianas para la bioproducción. La ingeniería metabólica de las levaduras, por ejemplo, es un área de rápido crecimiento en la biología de ingeniería para la producción sostenida de productos químicos, combustibles, alimentos y productos farmacéuticos.
Las levaduras tienen un potencial metabólico similar al de las células eucariotas y, por lo tanto, son más fáciles de modificar y cultivar a gran escala. Como resultado, los bioingenieros han diseñado y desarrollado sistemas CRISPR para levaduras.
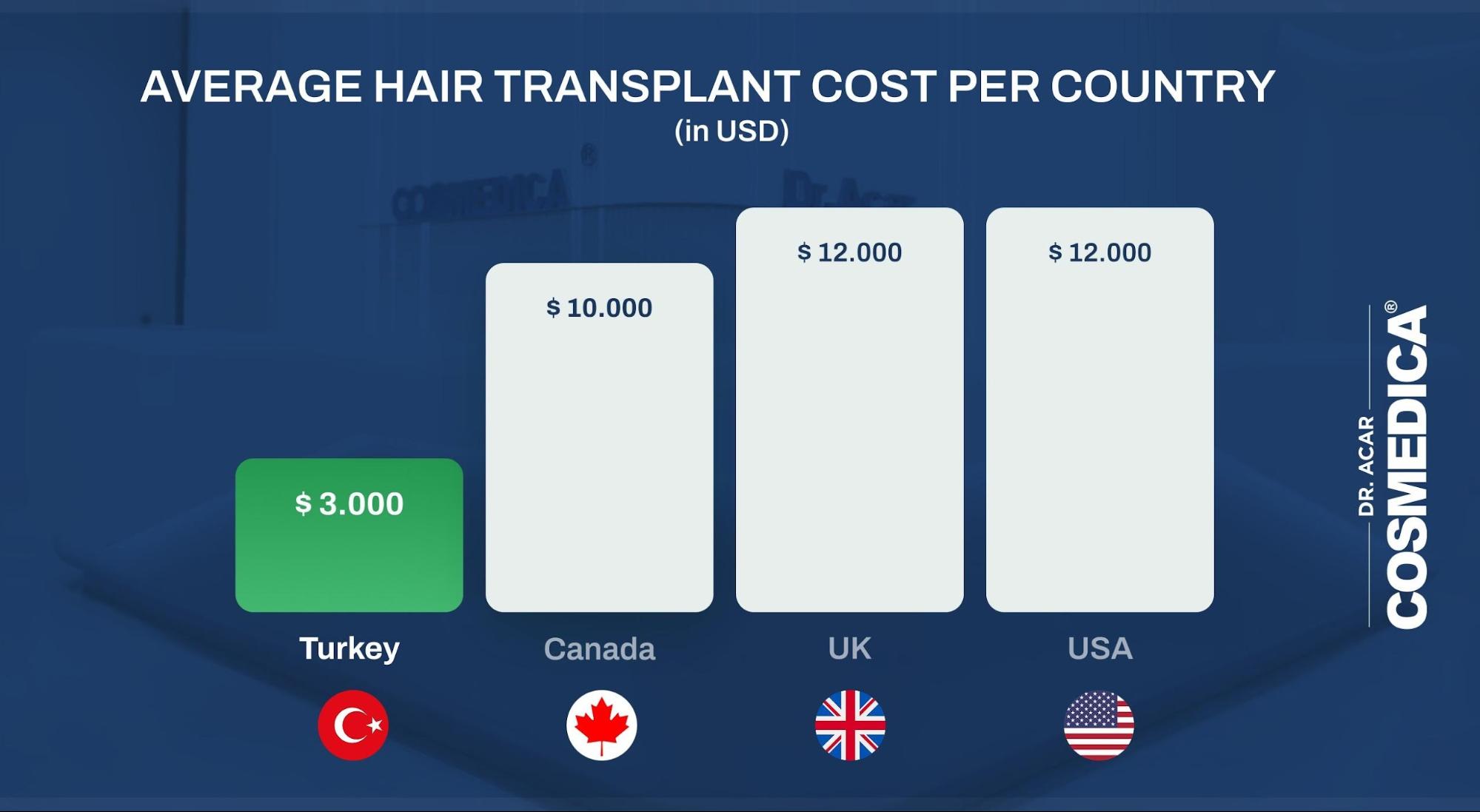
Debido a su alta eficiencia, CRISPR permite modificaciones genómicas sin marcadores. En este trabajo, Yuzbashev aseguró la optimización de cepas y facilitó proyectos de ingeniería metabólica mediante la identificación de tres mejoras en el sistema CRISPR/Cas9 para la ingeniería de levaduras. Los métodos incluyeron: 1) el intercambio fácil entre modificaciones con y sin marcador, 2) el intercambio rápido de brazos de homología para determinar diferentes ubicaciones de integración, y 3) un método sencillo para clonar gRNAs.
Para permitir la integración sin marcadores basada en CRISPR, el equipo eligió una rotura de doble cadena inducida por Cas9, que debía repararse para lograr la proliferación celular. Los científicos hicieron esto posible utilizando una plantilla o donante, integrada mediante recombinación homóloga o unión de extremos no homólogos (NHEJ), sin integración. El proceso de unión de extremos no homólogos se observa en la mayoría de las especies fúngicas, incluida la levadura de panadero Saccharomyces cerevisiae.
En especies con un mecanismo predominante de NHEJ, el equipo mejoró la recombinación homóloga mediante la eliminación de los genes de NHEJ. Si un método sin marcador no tuvo éxito, los científicos posteriormente buscaron mejorar la integración asistida por CRISPR-Cas9 para volver fácilmente a la integración basada en marcadores.
La integración asistida por Cas9 normalmente requiere una plantilla de donante que consiste en una cassette integrada flanqueada por dos brazos de homología. El equipo teorizó que la integración ideal de CRISPR/Cas9 debería intercambiar brazos de homología en construcciones de donantes de Cas9 preevaluadas a través de una reacción simplificada de ensamblaje Golden Gate.
Además, los promotores son un elemento clave en cualquier proyecto de ingeniería metabólica para redirigir el flujo hacia los productos de interés. Yuzbashev et al. utilizaron la levadura industrial Yarrowia lipolytica para desarrollar un kit de herramientas de ingeniería metabólica que combinaba estrategias de edición de genes y ensamblaje de ADN para lograr alta eficiencia y versatilidad.
Los científicos desbloquearon todo el potencial de CRISPR/Cas9 para la ingeniería metabólica mediante el desarrollo de un kit de herramientas que amplía los sistemas de ensamblaje Golden Gate previamente conocidos. Probaron el sistema de detección mediante la generación de varias bibliotecas de promotores. Yuzbashev et al. eligieron los genes ribosomales de Y. lipolytica que codifican proteínas de subunidades grandes y pequeñas. Identificaron una variedad de promotores con diversas fortalezas para ampliar el número de promotores para el mismo organismo.
Para demostrar la influencia y el uso del método mejorado de CRISPR/Cas9, el equipo creó una Y. lipolytica mediante ingeniería racional para producir ácido homogentísico (HGA). Típicamente, en condiciones alcalinas, el HGA se oxida espontáneamente para formar piorreumelanina autopolimerizada; un excelente componente de protectores solares naturales y cosméticos.
Despite its high commercial potential, existing methods to produce the acid precursor and pyomelanin product relied on the biotransformation of expensive aromatic amino acids. To facilitate metabolic engineering, the team therefore first selected several genes that encoded theprecursor aromatic aminotransferases as engineering targets. They then selected three overexpression targets to enhance the de novo synthesis of the homogentisic acid in the model organism. Finally, they studied and inactivated the HGA degradation pathway; a path yet unknown to exist in Y. lipolytica.
In this way, Tigran V. Yuzbashev and colleagues showed the dependence of metabolic engineering of living organisms on efficient DNA manipulation methods. This work presents an example of an enhanced molecular toolkit designed for CRISPR/Cas9-based metabolic engineering.
The scientists proved the functionality of the platform for both rapid strain construction and the characterization of a large library of promoters. They anticipate for this toolkit to have broader applications in strain engineering and in industry. The team envision for the Y. lipolytica model developed in this work to have overarching applications in other fields of biological engineering as well.
Guri Giaever et al, Functional profiling of the Saccharomyces cerevisiae genome, Nature (2002). DOI: 10.1038/nature00935
Journal information: Nature , Communications Biology
© 2023 Science X Network