Wissenschaftler züchten humanisierte Nieren in Schweineembryonen.
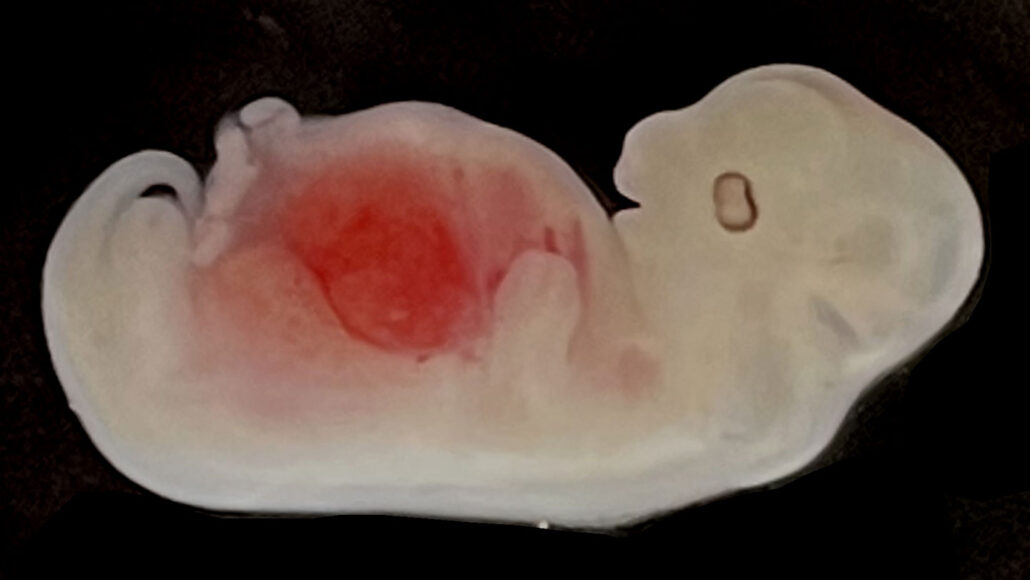
Wissenschaftlern ist es gelungen, Nieren, die hauptsächlich aus menschlichen Zellen bestehen, in Schweinembryonen zu züchten – was die Forscher zu einem weiteren Schritt auf dem langen Weg zur Erzeugung lebensfähiger menschlicher Organe für die Transplantation macht.
Die Ergebnisse, die am 7. September in Cell Stem Cell veröffentlicht wurden, markieren das erste Mal, dass ein solides humanisiertes Organ, eines mit menschlichen und tierischen Zellen, in einer anderen Spezies gezüchtet wurde.
„Dies ist ein erheblicher Fortschritt im Mensch-Tier-Chimärismus“, sagt Tao Tan, Zellbiologe an der Universität für Wissenschaft und Technologie Kunming in China, der 2021 bei der Schaffung des ersten chimären Mensch-Affen-Embryos mitgewirkt hat, an der aktuellen Entwicklung jedoch nicht beteiligt war Studie.
Allein in den Vereinigten Staaten stehen derzeit mehr als 100.000 Menschen auf einer Warteliste für Organtransplantationen. Die überwiegende Mehrheit dieser Menschen benötigt eine Nierentransplantation. Um diesen Bedarf an lebensrettenden Organtransplantationen zu decken, haben Wissenschaftler neue Methoden zur Züchtung von Organen und Geweben bei Tieren verfolgt (SN: 26.01.17).
Zu den Fortschritten der letzten Jahre zählen die Züchtung von Rattenorganen bei Mäusen (und umgekehrt) sowie die Vermenschlichung von Skelettmuskeln und Endothelgewebe bei Schweinen. Es bleiben jedoch erhebliche Hürden bestehen, die zum Teil darauf zurückzuführen sind, wie schwierig es für menschliche Zellen ist, in einem fremden Wirt zu gedeihen. Vom Menschen induzierte pluripotente Stammzellen (iPSCs), die als eine Art „Starterkit“ für die Züchtung vieler Arten menschlichen Gewebes fungieren, sterben oft ab, wenn sie in Tiere eingeführt werden, weil die Zellen der Spezies unterschiedliche physiologische Bedürfnisse haben.
Der Stammzellbiologe Liangxue Lai vom Guangzhou Institutes of Biomedicine and Health in China und sein Team haben mehr als fünf Jahre damit verbracht, ihre Methoden zu verfeinern, um die Überlebensfähigkeit menschlicher Stammzellen zu verbessern.
Während die Schweinembryonen noch nur einzelne Zellen waren, nutzte das Team das Genbearbeitungstool CRISPR/Cas9, um zwei für die Nierenentwicklung notwendige Gene herauszuschneiden. Dadurch entstand eine Nische, in der sich die menschlichen iPSCs, sobald sie in den Raum injiziert wurden, zu Nierenzellen entwickeln konnten. Die menschlichen Stammzellen wurden außerdem so optimiert, dass sie über besonders aktive Gene verfügen, die die Apoptose oder den Zelltod dämpfen, um die Zellen lange genug am Leben zu halten, um Fuß zu fassen und mit der Bildung der Niere zu beginnen.
Anschließend wurden mehr als 1.800 Embryonen auf Ersatzsauen übertragen, von denen fünf innerhalb der ersten 28 Tage für Studienzwecke entnommen wurden. Alle fünf hatten normale Nieren, die ihrem Entwicklungsstand entsprachen, und die Organe enthielten 50 bis 60 Prozent Zellen menschlichen Ursprungs. Das ist der höchste Anteil menschlicher Zellen, der bisher in einem Organ eines Schweins beobachtet wurde, sagt Tan. Mit mehr Zeit gebe es keinen Hinweis darauf, dass die Nieren nicht weiter wachsen und sich normal entwickeln würden, möglicherweise weil die menschlichen Zellen die Schweinezellen zunehmend verdrängen würden, sagen die Forscher.
Die Studie sei „ein wichtiger und interessanter Schritt“, sagt Massimo Mangiola, Transplantationsimmunologe an der New York University Langone Health, der nicht an der Forschung beteiligt war. Aber bis zu voll funktionsfähigen Xenotransplantationen seien es noch viele Jahre, stellt er fest.
Während sich die Stammzellen in mehrere Zelltypen differenzierten, darunter Nierenröhrenzellen und Entwicklungsgewebe, verfügt die menschliche Niere über mehr als 70 einzigartige Zelltypen, die Wissenschaftler rekapitulieren müssen. Und bis es den Forschern gelingt, ein zu 100 Prozent menschliches Organ zu schaffen, werden solche Transplantationen wahrscheinlich zu einer Abstoßung führen.
Darüber hinaus differenzierten sich einige iPSCs fälschlicherweise in Nervenzellen im Gehirn und Rückenmark der Embryonen. Mangiola sagt, dass die Zellen im Gegensatz zu den Nierenzellen zufällig zu sein scheinen, was ihn zu der Annahme veranlasst, dass sie wahrscheinlich nicht zu Tieren mit menschlichem Gehirn führen würden – was zu einem ethischen Dilemma führen würde.
Um solche ethischen Probleme zu vermeiden, wird das Team laut Lai in Zukunft Gene ausschalten, die die Differenzierung der Stammzellen in Neuronen steuern – sowie in Keimbahnzellen, Eier und Spermien, die genetische Informationen an die Nachkommen weitergeben. Das Team verfolgt außerdem die Züchtung anderer menschlicher Organvorläufer bei Schweinen, darunter das Herz und die Bauchspeicheldrüse.
„Wir haben das Gefühl, dass wir einen Meilenstein auf diesem Gebiet erreicht haben, aber dies ist nur der erste Schritt und es bleiben noch viele Herausforderungen“, sagt Lai. „Wir sind optimistisch, dass wir mit Zeit und Mühe auch diese Herausforderungen meistern können.“




