Wie Schnittameisen einen Pilzgarten anbauen, um Pflanzen abzubauen, könnte Einblicke in zukünftige Biokraftstoffe bieten.
1. Februar 2024
Dieser Artikel wurde gemäß dem redaktionellen Prozess und den Richtlinien von Science X überprüft. Die Herausgeber haben die folgenden Merkmale hervorgehoben, um die Glaubwürdigkeit des Inhalts sicherzustellen:
- faktengeprüft
- vertrauenswürdige Quelle
- lektoriert
von Maegan Murray, Pacific Northwest National Laboratory
Wissenschaftler haben Jahrzehnte damit verbracht, Wege zu finden, um Pflanzenmaterial effizient und kostengünstig abzubauen, so dass es in nützliche Bioprodukte umgewandelt werden kann, die den Alltag bereichern.
Biobasierte Kraftstoffe, Reinigungsmittel, Nahrungsergänzungsmittel und sogar Kunststoffe sind das Ergebnis dieser Arbeit. Und obwohl Wissenschaftler Möglichkeiten gefunden haben, Pflanzen so weit abzubauen, um eine Vielzahl von Produkten herzustellen, bleiben bestimmte Polymere wie Lignin, das eine Hauptkomponente der Zellwand von Pflanzen ist, unglaublich schwer in eine erschwingliche und umweltfreundliche Weise abzubauen, ohne dabei Schadstoffe in die Umwelt zurückzuführen. Diese Polymere können als Abfallprodukte zurückbleiben, die keinen weiteren Nutzen haben.
Eine spezialisierte Mikroben-Gemeinschaft bestehend aus Pilzen, Blattschneiderameisen und Bakterien ist bekannt dafür, Pflanzen auf natürliche Weise abzubauen und sie in Nährstoffe und andere Komponenten umzuwandeln, die von umgebenden Organismen und Systemen aufgenommen und genutzt werden. Aber die Identifizierung aller Komponenten und biochemischen Reaktionen, die für diesen Prozess benötigt werden, stellte bis jetzt eine bedeutende Herausforderung dar.
Kristin Burnum-Johnson, Leiterin der Wissenschaftsgruppe für funktionelle und systembiologische Forschung am Pacific Northwest National Laboratory (PNNL), und ein Team von PNNL-Forschern haben eine bildgebende Methode namens "Metabolome informed Proteome Imaging" (MIPI) entwickelt. Diese Methode ermöglicht es Wissenschaftlern, bis auf molekularer Ebene zu sehen, welche Basiskomponenten Teil des Pflanzenabbau-Prozesses sind und welche biochemischen Reaktionen wann und wo stattfinden, um ihn möglich zu machen.
Mit dieser Methode enthüllte das Team wichtige Metaboliten und Enzyme, die verschiedene biochemische Reaktionen antreiben, die für den Abbau-Prozess wichtig sind. Sie enthüllten auch den Zweck der residenten Bakterien im System - nämlich den Prozess noch effizienter zu machen. Diese Erkenntnisse können auf die zukünftige Entwicklung von Biokraftstoffen und Bioprodukten angewendet werden.
Die Forschung des Teams wurde kürzlich in Nature Chemical Biology veröffentlicht.
Symbiotische Beziehung zwischen Blattschneiderameisen und Pilz enthüllt Schlüssel zum Erfolg beim Abbau von Pflanzen
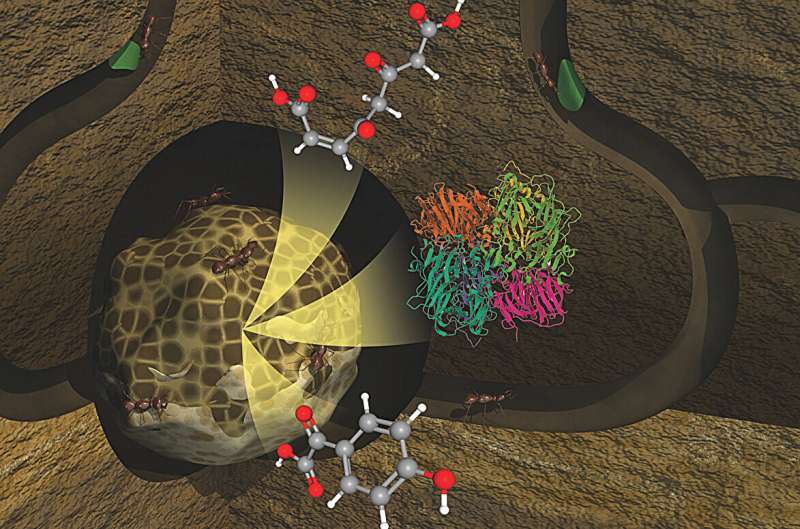
Für ihre Forschung untersuchte das Team eine Art von Pilz, der für seine symbiotische Beziehung mit einer Art von Blattschneiderameisen bekannt ist - ein Pilz namens Leucoagaricus gongylophorus. Die Ameisen nutzen den Pilz, um einen Pilzgarten anzulegen, der Pflanzenpolymere und andere Materialien abbaut. Überreste dieses Abbauprozesses werden von verschiedenen Organismen im Garten verwendet und konsumiert, so dass alle gedeihen können.
Die Ameisen vollenden diesen Prozess, indem sie den Pilz auf frischen Blättern in speziellen unterirdischen Strukturen anbauen. Diese Strukturen werden letztendlich zu den Pilzgärten, die das Material abbauen. Die residenten Bakterien unterstützen den Abbau, indem sie Aminosäuren und Vitamine produzieren, die das gesamte Gartensystem unterstützen.
'Umweltsysteme haben sich im Laufe von Millionen von Jahren zu perfekten symbiotischen Systemen entwickelt', sagte Burnum-Johnson. 'Wie können wir besser von diesen Systemen lernen, als zu beobachten, wie sie diese Aufgaben auf natürliche Weise bewältigen?'
Aber was diese Pilzgemeinschaft so schwierig zu untersuchen macht, ist ihre Komplexität. Während Pflanzen, Pilz, Ameisen und Bakterien alle aktive Bestandteile des Pflanzenabbau-Prozesses sind, konzentriert sich keiner von ihnen auf eine Aufgabe oder verbleibt an einem Ort. Wenn man dann noch die kleinskalige Größe der biochemischen Reaktionen auf molekularer Ebene berücksichtigt, ergibt sich ein unglaublich schwieriges Puzzle. Aber die neue MIPI-Bildgebungsmethode, die am PNNL entwickelt wurde, ermöglicht es Wissenschaftlern, genau zu sehen, was während des Abbau-Prozesses passiert.
'Wir haben jetzt die Werkzeuge, um die Feinheiten dieser Systeme vollständig zu verstehen und sie zum ersten Mal als Ganzes zu visualisieren', sagte Burnum-Johnson.
Mit Hilfe eines leistungsstarken Lasers nahm das Team Scans über 12 Mikrometer dicke Abschnitte eines Pilzgartens vor - ungefähr die Breite von Plastikfolie. Dieser Prozess half dabei, die Orte von Metaboliten in den Proben zu bestimmen, die Überreste von Pflanzenabbau sind. Diese Technik half auch dabei, den Ort und die Menge von Pflanzenpolymeren wie Zellulose, Xylan und Lignin sowie anderen Molekülen in spezifischen Regionen zu identifizieren. Die kombinierten Standorte dieser Komponenten deuteten auf Hotspots hin, an denen Pflanzenmaterial abgebaut worden war.
Von dort aus konzentrierte sich das Team auf diese Regionen, um Enzyme zu sehen, die verwendet werden, um biochemische Reaktionen in einem lebenden System anzustoßen. Das Wissen über Art und Ort dieser Enzyme ermöglichte es ihnen, festzustellen, welche Mikroben an diesem Prozess beteiligt waren.
All of these components together helped affirm the fungus as the primary degrader of the plant material in the system. Additionally, the team determined that the bacteria present in the system transformed previously digested plant polymers into metabolites that are used as vitamins and amino acids in the system. These vitamins and amino acids benefit the entire ecosystem by accelerating fungal growth and plant degradation.
Burnum-Johnson said if scientists had used other more traditional methods that take bulk measurements of primary components in a system, such as metabolites, enzymes, and other molecules, they would simply get an average of those materials, creating more noise and masking information.
'It dilutes the important chemical reactions of interest, often making these processes undetectable,' she said. 'To analyze the complex environmental ecosystems of these fungal communities, we need to know those fine detail interactions. These conclusions can then be taken back into a lab setting and used to create biofuels and bioproducts that are important in our everyday life.'
Marija Velickovic, a chemist and lead author of the paper, said she initially became interested in studying the fungal garden and how it degrades lignin based on the difficulty of the project.
'Fungal gardens are the most interesting because they are one of the most complex ecosystems composed of multiple members that effectively work together,' she said. 'I really wanted to map activities at the microscale level to better understand the role of each member in this complex ecosystem.'
Velickovic performed all the hands-on experiments in the lab, collecting material for the slides, scanning the samples to view and identify metabolites in each of the sections, and identifying hot spots of lignocellulose degradation.
Both Velickovic and Burnum-Johnson said they are ecstatic about their team's success.
'We actually accomplished what we set out for,' Burnum-Johnson said. 'Especially in science, that isn't guaranteed.'
The team plans to use its findings for further research, with specific plans to study how fungal communities respond and protect themselves amid disturbances and other perturbations.
'We now have an understanding of how these natural systems degrade plant material very well,' Burnum-Johnson said. 'By looking at complex environmental systems at this level, we can understand how they are performing that activity and capitalize on it to make biofuels and bioproducts.'
Provided by Pacific Northwest National Laboratory




